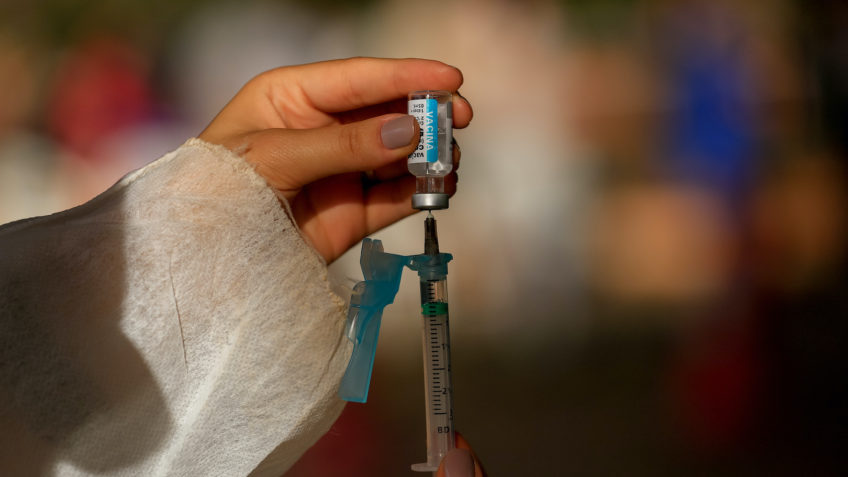
O 1º medicamento injetável de longa ação para prevenção do HIV começou a ser vendido no mercado privado brasileiro na 2ª feira (25.ago.2025). O fármaco é o cabotegravir, desenvolvido pela farmacêutica GSK e registrado pela Anvisa (Agência Nacional de Vigilância Sanitária) em 2023.
Comercializado sob o nome Apretude, o cabotegravir deve ser aplicado a cada 2 meses. Até agora, a única PrEP (profilaxia pré-exposição) disponível no Brasil era oferecida pelo SUS (Sistema Único de Saúde) desde 2017, mas em formato de comprimidos diários.
A PrEP é uma medicação preventiva indicada para pessoas com maior risco de entrar em contato com o HIV, vírus causador da Aids (estágio mais avançado da infecção). Incorporada ao SUS em 2017, a PrEP é distribuída gratuitamente na rede pública.
Segundo o Ministério da Saúde, foram registrados cerca de 46,5 mil novos casos de HIV em 2023. Projeções indicam que, mesmo com a PrEP oral já disponível, o país pode somar pelo menos 600 mil novos casos nos próximos 10 anos.
“Estamos trazendo ao Brasil a primeira PrEP injetável de longa ação, um avanço importante na prevenção ao HIV, com potencial para ampliar o acesso e beneficiar ainda mais a população do país”, disse Roberta Corrêa, diretora da Unidade de Negócios de HIV da GSK/ViiV Healthcare.
No Brasil, a incorporação do cabotegravir no SUS está em negociação. A análise de custo-benefício está a cargo da Conitec (Comissão Nacional de Incorporação de Tecnologias no SUS), vinculada ao Ministério da Saúde. O novo medicamento já pode ser adquirido em farmácias e clínicas, com opção de entrega direta ao paciente.
A principal vantagem das PrEP injetáveis está na maior adesão. Embora os comprimidos diários também reduzam o risco de infecção a quase 0, a exigência de uso contínuo ainda é vista como um entrave.
O setor já desenvolve soluções de proteção ainda mais prolongadas. Um exemplo é o lenacapavir, 1º medicamento injetável com duração de 6 meses. Sua comercialização foi aprovada pela EMA (Agência Europeia de Medicamentos) na 3ª feira (26.ago.2025) e pelos Estados Unidos em junho.
Em nota, a agência europeia afirmou que a PrEP é “um pilar no controle do HIV na Europa e no mundo”, mas destacou que a adesão “costuma ser inferior ao ideal”, seja por limitações de acesso, seja pela necessidade de administração diária em alguns tratamentos.